2023年11月份中美欧批准上市新药盘点
- 2024-01-16 09:22
- 作者:陈倩
- 来源:中国医药报
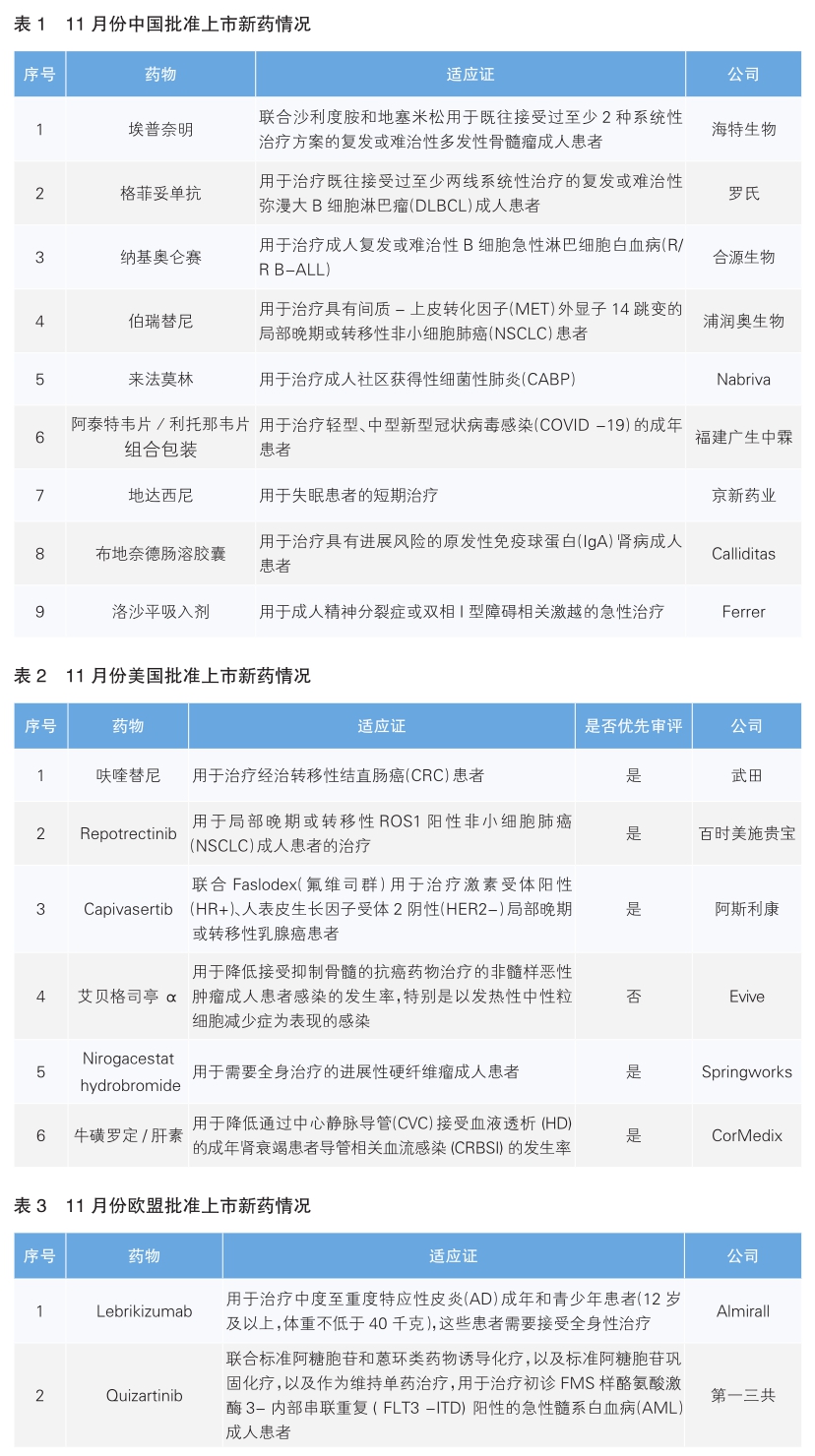
2023年11月份中美欧批准上市的新药中,共计有10款为全球范围内首次批准上市。其中,中国全球首次获批的新药数量最多,有5款;另外有两款国产创新药在美国获批上市。
我国批准9款新药上市
2023年11月份,我国批准了9款新药上市。根据Pharmadigger数据库,埃普奈明、纳基奥仑赛、伯瑞替尼、阿泰特韦/利托那韦片和地达西尼为全球范围内首次批准上市的新药。除地达西尼外,其余4款全为中国药企自主研发的新药。
埃普奈明是海特生物自主研发的重组变构人肿瘤坏死因子相关凋亡诱导配体,是目前全球唯一获批上市的死亡受体4(DR4)/DR5激动剂,通过外源性细胞凋亡途径触发细胞内Caspase级联反应,从而发挥抗肿瘤作用。该药本次获批是基于名为CPT-MM30的临床试验,结果显示,针对复发或难治性多发性骨髓瘤患者,埃普奈明联合沙利度胺和地塞米松具有明显的抗肿瘤活性,可以延长患者的无进展生存期及总生存期,并增加其总体缓解率。
格菲妥单抗是罗氏研发的同时靶向结合2种抗原分子(T细胞表面的CD3抗原和B细胞表面的CD20抗原)的双抗,独特的2∶1结构(2个CD20结合域和1个CD3结合域)赋予其更强的B细胞抓取能力和作用效力,尤其是针对弥漫性大B细胞淋巴瘤(DLBCL)这类起源于B淋巴细胞的肿瘤。该药本次获批主要是基于名为NP30179的Ⅱ期临床试验,结果显示,中位随访18.2个月后,经独立评审委员会(IRC)评估,患者完全缓解率(CR)达40%,有一半的患者能获得总体缓解。格菲妥单抗此前已于今年6月在美国获批上市。
纳基奥仑赛是合源生物自主研发的靶向CD19的CAR-T细胞治疗产品,是首款在中国获批上市的治疗白血病的CAR-T产品。该药此次获批基于一项纳基奥仑赛注射液用于治疗复发或难治性B细胞急性淋巴细胞白血病(R/R B-ALL)的单臂临床试验。试验结果显示,患者总体缓解率(ORR)达82.1%;在3个月时仍处于缓解的患者中,预计有80%的患者在1年时仍持续缓解。
伯瑞替尼是浦润奥生物自主研发的高选择性MET抑制剂。该药本次获批基于KUNPENG临床研究。研究结果显示,晚期MET14外显子跳跃突变非小细胞肺癌(NSCLC)患者接受治疗后,有3/4的患者获得客观缓解,中位无进展生存期(mPFS)达到12个月,中位缓解持续时间(mDOR)达到15.9个月。2021年12月,鞍石生物宣布完成对浦润奥生物的收购,从而将伯瑞替尼纳入了其研发管线。在中国以外的其它地区,伯瑞替尼的开发权益归冠科美博所有。
来法莫林最早由Nabriva Therapeutics公司研发,是一种创新截短侧耳素(pleuromutilin)类抗生素,与现有抗生素机制不同,不易产生耐药性和交叉耐药性。成人社区获得性肺炎是指在医院外罹患的肺实质炎症,包括具有明确潜伏期的病原体感染在入院后于潜伏期内发病的肺炎,是世界范围内发病率和病死率最高的疾病之一,是呼吸系统常见病、多发病。此前报告的在中国细菌性肺炎患者的Ⅲ期临床试验结果显示,来法莫林的疗效和安全性不劣于莫西沙星。该药此前已于2019年8月获批上市。
阿泰特韦片/利托那韦片组合包装是福建广生中霖生物科技有限公司自主研发的抗新冠病毒新药。阿泰特韦是一款高活性、高选择性的口服3CL蛋白酶抑制剂。3CL蛋白酶是新冠病毒复制必需的关键蛋白酶,在冠状病毒中高度保守,非药物诱导突变的自然发生概率较低,且没有人类同源蛋白,安全性良好。利托那韦主要用来抑制阿泰特韦代谢,从而升高阿泰特韦血药浓度,相当于增效剂。该药本次获批是基于在轻型/中型新冠患者中开展的Ⅱ/Ⅲ期临床试验。结果显示,阿泰特韦片/利托那韦片组相对于安慰剂组,患者所有新冠肺炎目标临床症状持续恢复中位时间缩短2天。
地达西尼是浙江京新药业研发的苯二氮卓类药物,通过部分激活γ-氨基丁酸A型(GABAA)受体,产生促进睡眠的作用。与已上市的治疗失眠类药物相比,地达西尼能选择性作用于GABAA受体α1亚基,既能迅速激活该受体并抑制神经系统活动,又能避免过度激活该受体而产生相关副作用。该药本次获批基于其Ⅲ期临床试验,结果显示,地达西尼对比安慰剂能快速起效、提高睡眠效率,同时改善次日嗜睡等残留效应。地达西尼最早由罗氏研发,后来Evotec获得了全球独占权并将其用于治疗失眠症。2010年,京新药业与Evotec签署协议,获得了地达西尼在中国的独家专利许可和开发权。
布地奈德肠溶胶囊是一款靶向肠道黏膜的免疫调节剂,通过特殊的制作工艺,将布地奈德靶向释放于回肠末端的黏膜B细胞。胶囊溶解后,三层包衣微丸持续稳定释放布地奈德,高浓度覆盖整个靶区域,从而减少诱发IgA肾病的半乳糖缺陷的IgA1抗体产生,进而干预发病机制上游阶段,达到治疗IgA肾病的作用。该药本次获批是基于一项Ⅲ期临床试验。试验结果显示,布地奈德肠溶胶囊能够保护肾功能,一定程度地减少肾功能衰退。布地奈德肠溶胶囊最初由Calliditas Therapeutics公司开发,云顶新耀拥有该产品在大中华区、新加坡和韩国的开发以及商业化权利。该药此前已于2021年在美国获批上市。
洛沙平是一种二环芳基类药物,主要被用于治疗精神分裂症等精神疾病,其主要作用机制为阻断多巴胺D2受体和血清素5-HT2受体,从而减轻精神分裂症患者的阳性症状,如幻觉、错觉和思维混乱等。此外,洛沙平也可能通过影响其他神经递质系统,如乙酰胆碱、组胺和肾上腺素等发挥作用。该药本次获批基于一项Ⅲ期临床试验,结果显示,洛沙平针对精神分裂症或双相情感障碍患者激越时显示急性控制,给药后两小时得出的阳性和阴性症状量表兴奋因子评分与基线的变化有显著统计差异。洛沙平吸入粉雾剂最初由Alexza公司开发,李氏大药厂拥有该药在中国的经销许可。该药此前已于2012年在美国获批上市。
美国批准6款新药上市
2023年11月份,美国批准了6款新药上市。根据Pharmadigger数据库信息,Repotrectinib、Capivasertib、Nirogacestat hydrobromide,以及牛磺罗定/肝素4款新药为全球首次获批;另外两款新药都来自中国药企,分别是呋喹替尼和艾贝格司亭α。
呋喹替尼是和记黄埔自主研发的一种选择性的口服抗血管内皮生长因子受体(VEGFR)-1、-2及-3的酪氨酸激酶抑制剂(TKI),是美国首个且唯一获批用于治疗经治转移性结直肠癌的针对全部三种VEGF受体激酶的高选择性抑制剂。武田拥有其在中国以外的全球范围内推进呋喹替尼针对所有适应证的开发、商业化和生产的独家许可。该药本次获批基于两项名为FRESCO和FRESCO-2的Ⅲ期临床试验,结果显示,呋喹替尼用药组患者的中位生存期比安慰剂组延长约2个月。该药此前已于2018年9月在中国上市。
Repotrectinib(Augtyro)是百时美施贵宝研发的靶向ROS1和NTRK的TKI(酪氨酸激酶抑制剂),本次获批主要是基于TRIDENT-1试验结果。结果显示,Repotrectinib在TKI初治和TKI经治的ROS1阳性NSCLC患者中,客观缓解率(ORR)均达到疗效终点。Repotrectinib最早由Turning Point公司开发;2020年7月,再鼎医药宣布与Turning Point公司达成合作,获得Repotrectinib在大中华区的独家开发及商业化权;2022年6月百时美施贵宝收购Turning Point公司。
Capivasertib是阿斯利康研发的三种AKT亚型(AKT1/2/3)的高效选择性抑制剂。AKT,也称为磷酸激酶B (PKB),在涉及细胞生长和分裂、细胞凋亡抑制和血管生成的多种级联信号传导机制中发挥着关键作用。该药本次获批是基于代号为CAPItello-291的Ⅲ期临床试验数据,在转移性乳腺癌患者中,Capivasertib+氟维司群组和安慰剂+氟维司群组的中位无进展生存期(PFS)分别为7.2个月和3.6个月,Capivasertib+氟维司群将患者疾病进展或死亡风险降低了40%。
艾贝格司亭α是亿帆医药控股子公司亿一生物(Evive Biotech)自主研发的集落刺激因子(G-CSF),是中国唯一一款同时在中国、美国获批的长效G-CSF药物。该药本次获批基于两项临床试验结果。在这两项试验中,艾贝格司亭α和化疗联用,与安慰剂或聚乙二醇非格司亭比较化疗引起的发热性中性粒细胞减少症的比例,结果显示,艾贝格司亭α疗效显著优于安慰剂,相较于聚乙二醇非格司亭疗效相当。艾贝格司亭α此前已于今年5月在中国获批上市。
牛磺罗定/肝素(DefenCath)是CorMedix公司研发的一种组合药物,是美国批准的第一个也是唯一一个抗菌导管封管解决方案。该组合药物本次获批是基于一项名为LOCK-IT-100的Ⅲ期临床试验。试验结果显示,与对照组肾衰竭患者相比,Def encath组患者的导管相关血流感染(CRBSI)事件发生率显著降低。
Nirogacestat hydrobromide(Ogsiveo)是Springworks公司研发的一款口服特异性γ-分泌酶小分子抑制剂,通过阻断Not ch受体的蛋白水解激活起作用,是首个被批准用于治疗硬纤维瘤的药物。该药本次获批基于在进展性硬纤维瘤患者中开展的Ⅲ期临床试验。试验结果显示,Nirogacestat相对于安慰剂用于进展性硬纤维瘤且无法接受手术的成年患者,患者的无进展生存期有显著提高。
欧盟批准2款新药上市
2023年11月份,欧盟批准了两款新药上市,根据Pharmadigger数据库,Lebrikizumab为全球首次批准。
Lebrikizumab(Ebglyss)由Almirall和礼来公司联合研发,是一种抗白介素13(IL-13)单克隆抗体,具有高亲和力,可以与可溶性I L-13结合,阻断IL-13信号通路。Almirall在欧洲拥有Lebrikizumab用于治疗皮肤病(包括特应性皮炎)的开发和商业化权利,而礼来公司则在欧洲以外的其他地区拥有独家开发和商业化权利。该药本次批准是基于三项Ⅲ期临床试验的结果,其中ADvocate 1和ADvocate 2评估了Lebrikizumab作为单药治疗的效果,而ADhere则评估了其与外用皮质类固醇(TCS)联合治疗的效果。结果显示,使用Lebrikizumab作为单药治疗的患者中,近60%患者实现了至少75%的疾病程度和严重性下降(EASI-75);而在与TCS联用时,有效性提高到了近70%。
Quizartinib(Vanflyta)是第一三共研发的一款口服的选择性第二代FLT3抑制剂,本次获批基于名为QuANTUM-First的Ⅲ期临床试验结果。在新诊断的FLT3-ITD阳性AML患者中,与标准化疗相比,Quizartinib可将患者死亡风险降低22%。Quizartinib此前已于2019年6月在日本获批上市,今年7月在美国获批上市。(陈倩)
(注:本文中的新药分别按中国、美国、欧盟三地新分子实体或生物药首次NDA/BLA来统计,一些药物首先在美国上市后首次在中国或欧盟上市时也会纳入统计)
《中国医药报》社版权所有,未经许可不得转载使用。
(责任编辑:陆悦)
分享至
右键点击另存二维码!
-
为你推荐