转化医学落到实处,胃癌免疫治疗一线审批全球共启
- 2021-01-21 22:25
- 作者:
- 来源:中国食品药品网
中国食品药品网讯 近日,国家药监局药品审评中心(CDE)官网公示:纳武利尤单抗注射液新适应证的上市申请已获正式受理,受理号为JXSS2000066、JXSS2000067。
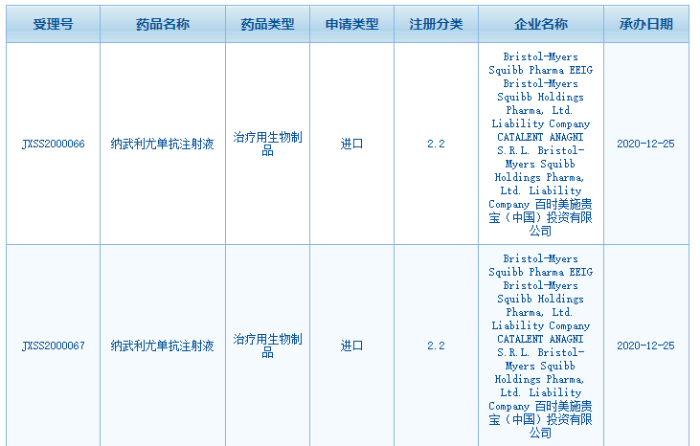
据悉,本次受理的纳武利尤单抗(俗称O药)的新适应证为晚期或转移性胃癌(GC)、胃食管连接部癌(GEJC)或食管腺癌(EAC)一线治疗。
基于一项全球多中心关键性Ⅲ期临床研究CheckMate-649的无进展生存期(PFS)和总生存期(OS)双优效结果,O药的胃癌、胃食管连接部癌及食管腺癌一线治疗适应证的上市注册申报日前已在全球包括美国、加拿大、瑞士、澳大利亚、巴西、中国、欧盟在内的多个国家和地区同步进行中。昨日最新消息,美国食品和药品管理局(FDA)已接受补充生物制品许可申请(sBLA),同时授予这一申请优先审评资格,预计在今年5月25日前做出回复。
此外,基于另一项主要在日本、韩国和中国台湾开展的ATTRACTION-4研究的PFS显著获益结果,O药的胃癌一线适应证也已在日本递交。
在各国近乎同步开展胃癌一线适应证的审批“大动作下”,O药能否成为首个在全球主要国家和地区同期获批同一适应证的PD-1抑制剂?
中国胃癌年死亡占全球一半,“缺药少药”是痛点
纵观全球的胃癌数据,亚洲一直位居前列,其中中国较为严峻。在庞大的人口基数和特色的饮食习惯下,胃癌在中国已成为仅次于肺癌的第二大瘤种,中国胃癌的发病率与死亡率均占全球50%左右 。
更令人担忧的是,80%的中国患者在初次诊断时往往已至中晚期,失去了通过手术根治的机会。由于很多晚期或转移性胃癌患者会因为病情恶化无法耐受后续治疗,所以一线治疗是决定患者生存获益和后续治疗效果的关键因素。
此外,十年来,除了HER2靶向药,晚期胃癌一线药物治疗始终没有取得进展。且在中国,HER2阳性的患者仅占12%~13% 。所以,化疗仍是大部分晚期胃癌患者的标准一线治疗方法,通常只能给患者带来不足1年的生存获益 。
在胃癌高发病率、高死亡率又缺药少药的境况下,这几年在肺癌、黑色素瘤、霍奇金淋巴瘤、食管癌等瘤种治疗中为患者带来显著生存获益的PD-1抑制剂被寄予厚望。
据了解,国产的PD-1抑制剂在胃癌一线方面还没有Ⅲ期的临床研究数据发布。多个进口的PD-1/PD-L1抑制剂虽已陆续发布研究结果,但目前达到临床研究终点的只有O药联合化疗的CheckMate-649和ATTRACTION-4研究。其中,CheckMate-649研究是目前唯一在胃癌一线领域达到OS与PFS双终点的临床研究。
CheckMate-649研究纳入大规模中国胃癌患者,证实生存获益显著
胃癌具有高度异质性,东西方人群在发病特征、生物学行为、治疗模式上都存在较大差异。
针对这一问题,CheckMate-649研究纳入了几乎遍及全球的试验中心,成为迄今为止在胃癌与食管腺癌领域开展的规模最大的随机对照、全球Ⅲ期临床研究。大样本量囊括了东西方各种胃癌类型,均匀覆盖了研究所需的分子分型,并考虑了胃癌治疗的高度异质性难题。
此外,在已公布数据结果的胃癌免疫治疗研究中,CheckMate-649是首个纳入中国大陆人群的全球多中心Ⅲ期研究;中国患者数量在入组的亚洲患者中占比最高,达60%。通过研究设计可以发现,联合方案的策略高度吻合目前中国临床实践,分层因素考虑了临床相关预后因素,入组的患者特征具备一线胃癌的疾病代表性,且基线临床特征分布均衡,这些对中国人群的获益风险评估提供了稳健的基础。
根据2020年ESMO公布的CheckMate-649研究中纳武利尤单抗+化疗对比单独化疗的中期数据结果 ,纳武利尤单抗联合化疗成功跨越了化疗普遍生存不足1年的“坎”。研究结果所显示出的令人惊喜的生存曲线,为未来的胃癌一线治疗注入了信心,也有望改写胃癌一线治疗的新标准。而下一步,大家最为关心的是患者何时才能真正地用上这对“黄金组合”?
“中国速度”以患者为先,更多胃癌患者有望获益于创新药
新医改进行十余年来,我国新药审批速度不断提升,进口药在中国的获批时间逐年缩短。2017年,随着《关于深化审评审批制度改革鼓励药品医疗器械创新的意见》出台,包含人种差异数据的全球临床试验数据已获得我国进口药申报和审批流程的认可,进口药上市速度得到进一步提升。
在国际方面,如今药物审批步伐的一致性与快速性倚赖于全球药监机构之间充分的数据信息与意见沟通协作,因而得以尽快满足患者的救治需求。
获益于新药审评审批的加快,基于中国台湾人群的显著生存获益数据,O药的胃或胃食管连接部腺癌三线适应证已于2020年3月在中国获批,突破了中国晚期胃癌治疗“后线缺药”的僵局。
而胃癌一线治疗是患者取得疗效的最佳机会,随着CheckMate-649研究的突破性成功,相信“中国速度”将造福更多中国胃癌患者。
《中国医药报》社版权所有,未经许可不得转载使用。
(责任编辑:张可欣)
分享至
右键点击另存二维码!
-
为你推荐